Σωμάτιο Μπαρ

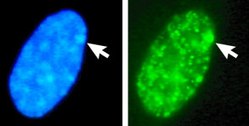
Το σωμάτιο Μπαρ (Barr) (πήρε το όνομά του από τον Murray Barr)[1] ή χρωματίνη Χ είναι ένα ανενεργό Χρωμόσωμα Χ. Σε είδη με καθορισμό φύλου XY (συμπεριλαμβανομένων των ανθρώπων), τα θηλυκά έχουν συνήθως δύο χρωμοσώματα Χ,[2] και το ένα καθίσταται ανενεργό σε μια διαδικασία που ονομάζεται υπόθεση της Lyon (lyonization). Τα σφάλματα στον διαχωρισμό των χρωμοσωμάτων μπορεί επίσης να οδηγήσουν σε αρσενικά και θηλυκά άτομα με επιπλέον χρωμοσώματα Χ. Η υπόθεση της Λυών δηλώνει ότι σε κύτταρα με πολλαπλά χρωμοσώματα Χ, όλα εκτός από ένα απενεργοποιούνται νωρίς στην εμβρυϊκή ανάπτυξη στα θηλαστικά.[3][4] Τα χρωμοσώματα Χ που αδρανοποιούνται επιλέγονται τυχαία, εκτός από τα μαρσιποφόρα και σε ορισμένους εξωεμβρυϊκούς ιστούς ορισμένων πλακουντοφόρων θηλαστικών, στους οποίους το χρωμόσωμα Χ από το σπέρμα είναι πάντα απενεργοποιημένο.[5] Σε ανθρώπους με ευπλοειδία, ένα γονοτυπικό θηλυκό (καρυότυπος 46, XX) έχει ένα σωμάτιο Barr ανά σωματικό κυτταρικό πυρήνα, ενώ ένα γονοτυπικό αρσενικό (46, XY) δεν έχει κανένα. Το σωματίδιο Barr μπορεί να φανεί στον μεσοφασικό πυρήνα ως μια σκούρα χρωματισμένη μικρή μάζα σε επαφή με τη μεμβράνη του πυρήνα. Τα σωμάτια Barr μπορούν να παρατηρηθούν στα ουδετερόφιλα στο χείλος του πυρήνα. Σε ανθρώπους με περισσότερα από ένα χρωμοσώματα Χ, ο αριθμός των σωμάτιων Barr που είναι ορατά στη μεσόφαση είναι πάντα ένα λιγότερο από τον συνολικό αριθμό των χρωμοσωμάτων Χ. Για παράδειγμα, τα άτομα με σύνδρομο Klinefelter (47, XXY) έχουν ένα μόνο σωμάτιο Barr και τα άτομα με καρυότυπο (47, XXX) έχουν δύο σωμάτια Barr.
Μηχανισμός
[Επεξεργασία | επεξεργασία κώδικα]Κάποιος με δύο χρωμοσώματα Χ (όπως η πλειονότητα των ανθρώπινων θηλυκών) έχει μόνο ένα σώμα Barr ανά σωματικό κύτταρο, ενώ κάποιος με ένα χρωμόσωμα Χ (όπως οι περισσότεροι άνδρες) δεν έχει κανένα. Η αδρανοποίηση του χρωμοσώματος Χ των θηλαστικών ξεκινά από το κέντρο αδρανοποίησης Χ (X inactivation centre, Xic), που συνήθως βρίσκεται κοντά στο κεντρομερίδιο.[6] Το κέντρο περιέχει δώδεκα γονίδια, επτά από τα οποία κωδικοποιούν πρωτεΐνες, πέντε για αμετάφραστα RNA, από τα οποία μόνο δύο είναι γνωστό ότι παίζουν ενεργό ρόλο στη διαδικασία αδρανοποίησης του X, το Χ-αδρανές ειδικό μεταγράφημα (X-inactive specific transcript, Xist) και το Tsix (αντινοηματικό του Xist).[6] Το κέντρο φαίνεται επίσης να είναι σημαντικό στη μέτρηση των χρωμοσωμάτων: διασφαλίζοντας ότι η τυχαία αδρανοποίηση λαμβάνει χώρα μόνο όταν υπάρχουν δύο ή περισσότερα χρωμοσώματα Χ. Η παροχή ενός επιπλέον τεχνητού "Xic" στην πρώιμη εμβρυογένεση μπορεί να προκαλέσει αδρανοποίηση του μοναδικού Χ που βρίσκεται στα αρσενικά κύτταρα.[6] Οι ρόλοι του Xist και του Tsix φαίνεται να είναι ανταγωνιστικοί. Η απώλεια της έκφρασης Tsix στο μελλοντικό ανενεργό χρωμόσωμα Χ οδηγεί σε αύξηση των επιπέδων του Xist γύρω από το Xic. Εν τω μεταξύ, στο μελλοντικό ενεργό X τα επίπεδα Tsix διατηρούνται. Έτσι τα επίπεδα του Xist παραμένουν χαμηλά.[7] Αυτή η μετατόπιση επιτρέπει στο "Xist" να αρχίσει να επικαλύπτει το μελλοντικό ανενεργό χρωμόσωμα, που εξαπλώνεται από το "Xic".[2] Στη μη τυχαία αδρανοποίηση αυτή η επιλογή φαίνεται να είναι σταθερή και τα τρέχοντα στοιχεία υποδηλώνουν ότι το γονίδιο που κληρονομείται από τη μητέρα μπορεί να είναι αποτυπωμένο.[3] Διακυμάνσεις στη συχνότητα Xi έχουν αναφερθεί με την ηλικία, την εγκυμοσύνη, τη χρήση από του στόματος αντισυλληπτικών, τις διακυμάνσεις του εμμηνορροϊκού κύκλου και τη νεοπλασία.[8] Θεωρείται ότι αυτό αποτελεί τον μηχανισμό επιλογής και επιτρέπει στις κατάντη διεργασίες να καθορίσουν τη συμπαγή κατάσταση του σωμάτιου Barr. Αυτές οι αλλαγές περιλαμβάνουν τροποποιήσεις ιστόνης, όπως η μεθυλίωση της ιστόνης H3 (δηλαδή H3K27me3 από PRC2 που στρατολογείται από το Xist)[9] ουβικουϊτινοποίηση της ιστόνης H2A,[10] καθώς και άμεση τροποποίηση του ίδιου του DNA, μέσω της μεθυλίωσης των θέσεων CpG.[11] Αυτές οι αλλαγές βοηθούν στην αδρανοποίηση της έκφρασης του γονιδίου στο ανενεργό χρωμόσωμα Χ και στη συμπίεσή του για να σχηματιστεί το σωμάτιο Barr. Η επανενεργοποίηση ενός σωματίου Barr είναι επίσης δυνατή και έχει παρατηρηθεί σε ασθενείς με καρκίνο του μαστού.[12] Μια μελέτη έδειξε ότι η συχνότητα των σωματίων Barr στο καρκίνωμα του μαστού ήταν σημαντικά χαμηλότερη από ό,τι σε υγιείς μάρτυρες, υποδεικνύοντας την επανενεργοποίηση αυτών των χρωμοσωμάτων Χ που μόλις απενεργοποιήθηκαν.[12]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Barr, M. L.; Bertram, E. G. (1949). «A Morphological Distinction between Neurones of the Male and Female, and the Behaviour of the Nucleolar Satellite during Accelerated Nucleoprotein Synthesis». Nature 163 (4148): 676–677. doi:. PMID 18120749. Bibcode: 1949Natur.163..676B.
- ↑ 2,0 2,1 Lyon, M. F. (2003). «The Lyon and the LINE hypothesis». Seminars in Cell & Developmental Biology 14 (6): 313–318. doi:. PMID 15015738.
- ↑ 3,0 3,1 Brown, C.J., Robinson, W.P., (1997), XIST Expression and X-Chromosome Inactivation in Human Preimplantation Embryos Am. J. Hum. Genet. 61, 5–8 (Full Text PDF)
- ↑ Lyon, M. F. (1961). «Gene Action in the X-chromosome of the Mouse (Mus musculus L.)». Nature 190 (4773): 372–373. doi:. PMID 13764598. Bibcode: 1961Natur.190..372L.
- ↑ Lee, J. T. (2003). «X-chromosome inactivation: a multi-disciplinary approach». Seminars in Cell & Developmental Biology 14 (6): 311–312. doi:. PMID 15015737.
- ↑ 6,0 6,1 6,2 Rougeulle, C.; Avner, P. (2003). «Controlling X-inactivation in mammals: what does the centre hold?». Seminars in Cell & Developmental Biology 14 (6): 331–340. doi:. PMID 15015740.
- ↑ Lee, J. T.; Davidow, L. S.; Warshawsky, D. (1999). «Tisx, a gene antisense to Xist at the X-inactivation centre». Nat. Genet. 21 (4): 400–404. doi:. PMID 10192391.
- ↑ Sharma, Deepti (January 10, 2018). «Deciphering the Role of the Barr Body in Malignancy». Sultan Qaboos University Medical Journal 17 (4): 389–397. doi:. PMID 29372079.
- ↑ Heard, E.; Rougeulle, C.; Arnaud, D.; Avner, P.; Allis, C. D. (2001). «Methylation of Histone H3 at Lys-9 Is an Early Mark on the X Chromosome during X Inactivation». Cell 107 (6): 727–738. doi:. PMID 11747809.
- ↑ de Napoles, M.; Mermoud, J.E.; Wakao, R.; Tang, Y.A.; Endoh, M.; Appanah, R.; Nesterova, T.B.; Silva, J. και άλλοι. (2004). «Polycomb Group Proteins Ring1A/B Link Ubiquitylation of Histone H2A to Heritable Gene Silencing and X Inactivation». Dev. Cell 7 (5): 663–676. doi:. PMID 15525528.
- ↑ Chadwick, B.P.; Willard, H.F. (2003). «Barring gene expression after XIST: maintaining faculative heterochromatin on the inactive X.». Seminars in Cell & Developmental Biology 14 (6): 359–367. doi:. PMID 15015743.
- ↑ 12,0 12,1 Natekar, Prashant E.; DeSouza, Fatima M. (2008). «Reactivation of inactive X chromosome in buccal smear of carcinoma of breast». Indian Journal of Human Genetics 14 (1): 7–8. doi:. ISSN 0971-6866. PMID 20300284.
Παραπέρα μελέτη
[Επεξεργασία | επεξεργασία κώδικα]- Alberts, B.· Johnson, A.· Lewis, J.· Raff, M.· Roberts, K.· Walter, P. (2002). Molecular Biology of the Cell, Fourth Edition. Garland Science. σελίδες 428–429. ISBN 978-0-8153-4072-0. (Web Edition, Free access)
- Turnpenny & Ellard: Emery's Elements of Medical Genetics 13E (http://www.studentconsult.com/content/default.cfm?ISBN=9780702029172&ID=HC006029 Αρχειοθετήθηκε 2020-04-13 στο Wayback Machine.)
