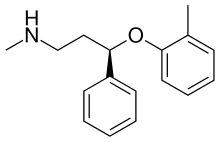
Ατομοξετίνη
 | |
 | |
| Ονομασία IUPAC | |
|---|---|
(3R)-N-Methyl-3-(2-methylphenoxy)-3-phenylpropan-1-amine | |
| Κλινικά δεδομένα | |
| Εμπορικές ονομασίες | Strattera, άλλες |
| AHFS/Drugs.com | monograph |
| MedlinePlus | a603013 |
| Δεδομένα άδειας |
|
| Κατηγορία ασφαλείας κύησης | |
| Οδοί χορήγησης | Από το στόμα |
| Κυκλοφορία | |
| Κυκλοφορία |
|
| Φαρμακοκινητική | |
| Βιοδιαθεσιμότητα | 63 με 94%[2][3][4] |
| Πρωτεϊνική σύνδεση | 98%[2][3][4] |
| Μεταβολισμός | Ήπαρ, μέσω του CYP2D6[2][3][4] |
| Βιολογικός χρόνος ημιζωής | 4,5-19 ώρες[2][3][4][5][6] |
| Απέκκριση | Νεφρά (80%) και κόπρανα (17%)[2][3][4] |
| Κωδικοί | |
| Αριθμός CAS | 83015-26-3 |
| Κωδικός ATC | N06BA09 |
| PubChem | CID 54841 |
| IUPHAR/BPS | 7118 |
| DrugBank | DB00289 |
| ChemSpider | 49516 |
| UNII | ASW034S0B8 |
| KEGG | D07473 |
| ChEBI | CHEBI:127342 |
| ChEMBL | CHEMBL641 |
| Συνώνυμα | (R)-N-Methyl-3-phenyl-3-(o-tolyloxy)propan-1-amine |
| Χημικά στοιχεία | |
| Χημικός τύπος | C17H21NO |
| Μοριακή μάζα | 255,36 g·mol−1 |
CC1=C(C=CC=C1)O[C@H](CCNC)C2=CC=CC=C2 | |
InChI=1S/C17H21NO/c1-14-8-6-7-11-16(14)19-17(12-13-18-2)15-9-4-3-5-10-15/h3-11,17-18H,12-13H2,1-2H3/t17-/m1/s1 Key:VHGCDTVCOLNTBX-QGZVFWFLSA-N | |
| (verify) | |
Η ατομοξετίνη, που πωλείται με το εμπορικό σήμα Strattera μεταξύ άλλων, είναι φάρμακο που χρησιμοποιείται για τη θεραπεία της διαταραχής έλλειψης προσοχής-υπερκινητικότητας (ΔΕΠΥ).[7] Μπορεί να χρησιμοποιηθεί μόνο του ή μαζί με ψυχοδιεγερτικά.[8][9] Η χρήση της ατομοξετίνης συνιστάται μόνο σε άτομα ηλικίας τουλάχιστον έξι ετών. Λαμβάνεται από το στόμα. Εγκρίθηκε για ιατρική χρήση στις Ηνωμένες Πολιτείες το 2002. Το 2018, ήταν το 162ο πιο συχνά συνταγογραφούμενο φάρμακο στις Ηνωμένες Πολιτείες, με περισσότερα από 3 εκατομμύρια συνταγές.[10][11]
Οι συχνές ανεπιθύμητες ενέργειες της ατομοξετίνης περιλαμβάνουν κοιλιακό άλγος, απώλεια όρεξης, ναυτία, αίσθημα κόπωσης και ζάλη.[7] Οι σοβαρές ανεπιθύμητες ενέργειες μπορεί να περιλαμβάνουν αγγειοοίδημα, ηπατικά προβλήματα, εγκεφαλικό επεισόδιο, ψύχωση, καρδιακά προβλήματα, αυτοκτονία και επιθετικότητα.[12] Δεν υπάρχουν επαρκή δεδομένα σχετικά με την ασφάλειά της κατά τη διάρκεια της εγκυμοσύνης. Όσον αφορά το 2019, η ασφάλειά της κατά τη διάρκεια της εγκυμοσύνης και για χρήση κατά τη διάρκεια του θηλασμού δεν είναι σίγουρη.[13][14]
Η ατομοξετίνη είναι αναστολέας επαναπρόσληψης νορεπινεφρίνης και πιστεύεται ότι δρα αυξάνοντας τα επίπεδα νορεπινεφρίνης και ντοπαμίνης στον εγκέφαλο.[7][5]
Ιατρικές χρήσεις
[Επεξεργασία | επεξεργασία κώδικα]Διαταραχή ελλειμματικής προσοχής-υπερκινητικότητας
[Επεξεργασία | επεξεργασία κώδικα]Η ατομοξετίνη έχει εγκριθεί για χρήση σε παιδιά, εφήβους και ενήλικες.[15] Ωστόσο, η αποτελεσματικότητά του δεν έχει μελετηθεί σε παιδιά κάτω των έξι ετών.[3] Το πρωταρχικό πλεονέκτημά του έναντι των τυπικών διεγερτικών θεραπειών για ΔΕΠΥ είναι ότι έχει ελάχιστα γνωστό δυναμικό κατάχρησης. Ενώ έχει αποδειχθεί ότι μειώνει σημαντικά τα έλλειψης προσοχής και υπερκινητικά συμπτώματα, οι αποκρίσεις ήταν χαμηλότερες από την απόκριση στα διεγερτικά. Επιπλέον, το 40% των συμμετεχόντων που έλαβαν ατομοξετίνη εμφάνισαν υπολειμματικά συμπτώματα ΔΕΠΥ.[16]
Ενώ η αποτελεσματικότητά του μπορεί να είναι μικρότερη από εκείνη των διεγερτικών φαρμάκων,[17] υπάρχουν κάποιες ενδείξεις ότι μπορεί να χρησιμοποιηθεί σε συνδυασμό με διεγερτικά.[8] Οι γιατροί μπορεί να συνταγογραφήσουν μη διεγερτικά συμπεριλαμβανομένης της ατομοξετίνης όταν ένα άτομο έχει ενοχλητικές παρενέργειες από τα διεγερτικά, όταν ένα διεγερτικό δεν ήταν αποτελεσματικό, σε συνδυασμό με ένα διεγερτικό για την αύξηση της αποτελεσματικότητας,[18][19] ή όταν υπάρχει ανησυχία για το δυναμικό κατάχρησης ψυχοδιεγερτικών σε έναν ασθενή με ιστορικό διαταραχής χρήσης ναρκωτικών.
Σε αντίθεση με τους αγωνιστές α2 αδρενοϋποδοχέα όπως η γουανφασίνη και κλονιδίνη, η χρήση ατομοξετίνης μπορεί να σταματήσει απότομα χωρίς να παρατηρηθούν σημαντικές επιδράσεις λόγω της διακοπής.[3]
Οι αρχικές θεραπευτικές επιδράσεις της ατομοξετίνης χρειάζονται συνήθως 2-4 εβδομάδες για να γίνουν εμφανείς. Ενδέχεται να απαιτηθούν άλλες 2–4 εβδομάδες για να επιτευχθούν τα πλήρη θεραπευτικά αποτελέσματα.[20] Η μέγιστη συνιστώμενη συνολική ημερήσια δόση σε παιδιά και εφήβους άνω των 70 ετών κιλά και ενήλικες είναι 100 mg.[15]
Άλλες
[Επεξεργασία | επεξεργασία κώδικα]Η ατομοξετίνη μπορεί να χρησιμοποιηθεί σε άτομα με ΔΕΠΥ και διπολική διαταραχή αν και τέτοια χρήση δεν έχει μελετηθεί καλά.[21] Κάποιο όφελος έχει επίσης παρατηρηθεί σε άτομα με ΔΕΠΥ και αυτισμό.[22]
Έχει προταθεί ότι η ατομοξετίνη μπορεί να είναι χρήσιμο συμπλήρωμα σε άτομα με μείζονα κατάθλιψη, ιδιαίτερα σε περιπτώσεις με ταυτόχρονη ΔΕΠΥ.[23]
Αντενδείξεις
[Επεξεργασία | επεξεργασία κώδικα]Οι αντενδείξεις περιλαμβάνουν:[3]
- Υπερευαισθησία στην ατομοξετίνη ή σε κάποιο από τα ανενεργά συστατικά του προϊόντος
- Συμπτωματική καρδιαγγειακή νόσος όπως:
- -μέτρια προς σοβαρή υπέρταση
- -κολπική μαρμαρυγή
- -κολπικός πτερυγισμός
- -κοιλιακή ταχυκαρδία
- -κοιλιακή μαρμαρυγή
- -κοιλιακός πτερυγισμός
- -προχωρημένη αρτηριοσκλήρυνση
- Σοβαρές καρδιαγγειακές νόσοι
- Φαιοχρωμοκύτωμα
- Ταυτόχρονη θεραπεία με αναστολείς μονοαμινοξειδάσεις (ΜΑΟ)
- Γλαύκωμα κλειστής γωνίας
- Κακοί μεταβολίτες (εξαιτίας του μεταβολισμού της ατομοξετίνης από το CYP2D6)
Παρενέργειες
[Επεξεργασία | επεξεργασία κώδικα]Συχνές ανεπιθύμητες ενέργειες περιλαμβάνουν κοιλιακό άλγος, απώλεια όρεξης, ναυτία, αίσθημα κόπωσης και ζάλη.[7] Οι σοβαρές ανεπιθύμητες ενέργειες μπορεί να περιλαμβάνουν αγγειοοίδημα, ηπατικά προβλήματα, εγκεφαλικό επεισόδιο, ψύχωση, καρδιακά προβλήματα, αυτοκτονία και επιθετικότητα.[12] Μια μετα-ανάλυση του 2020 διαπίστωσε ότι η ατομοξετίνη συσχετίστηκε με ανορεξία, απώλεια βάρους και υπέρταση, χαρακτηρίζοντάς την ως «δυνητικά λιγότερο προτιμώμενος παράγοντας με βάση την ασφάλεια» για τη θεραπεία της ΔΕΠΥ.[24] Όσον αφορά το 2019, η ασφάλεια κατά την εγκυμοσύνη και τον θηλασμό δεν είναι σαφής.[13] μια ανασκόπηση του 2018 δήλωσε ότι, "[β] λόγω έλλειψης δεδομένων, ο θεράπων ιατρός θα πρέπει να εξετάσει το ενδεχόμενο διακοπής της θεραπείας με ατομοξετίνη σε γυναίκες με ADHD κατά τη διάρκεια της εγκυμοσύνης."[14]
Η Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων (FDA) εξέδωσε προειδοποίηση μαύρου κουτιού για αυτοκτονική συμπεριφορά / ιδεασμό. Παρόμοιες προειδοποιήσεις έχουν εκδοθεί στην Αυστραλία.[3][25] Σε αντίθεση με τα διεγερτικά φάρμακα, η ατομοξετίνη δεν έχει δυναμικό κατάχρησης ή τη δυνατότητα να προκαλέσει αποτελέσματα απόσυρσης στην απότομη διακοπή.
Επίπτωση ανεπιθύμητων ενεργειών:[3][26][27]
Πολύ συχνές (> 10% επίπτωση) ανεπιθύμητες ενέργειες περιλαμβάνουν:
- Ναυτία (26%)
- Ξηροστομία (20%)
- Απώλεια όρεξης (16%)
- Αϋπνία (15%)
- Κόπωση (10%)
- Πονοκέφαλος
- Βήχας
- Έμετος (σε παιδιά και εφήβους)
Οι συχνές ανεπιθύμητες ενέργειες (επίπτωση 1-10%) περιλαμβάνουν:
- Δυσκοιλιότητα (8%)
- Ζάλη (8%)
- Στυτική δυσλειτουργία (8%)
- Υπνηλία (8%)
- Κοιλιακός πόνος (7%)
- Ντροπαλή κύστη (6%)
- Ταχυκαρδία (5–10%)
- Υπέρταση (5–10%)
- Ευερεθιστότητα (5%)
- Αφύσικα όνειρα (4%)
- Δυσπεψία (4%)
- Διαταραχές εκσπερμάτωσης (4%)
- Υπεριδρωσία (αυξημένη παραγωγή ιδρώτα) (4%)
- Εμετοί (4%)
- Εξάψεις (3%)
- Παραισθησία (3%)
- Διαταραχές εμμήνου ρύσεως (3%)
- Απώλεια βάρους (2%)
- Κατάθλιψη
- Δερματίτιδα
- Αλλαγές διάθεσης
Όχι συχνές (0,1-1% επίπτωση) ανεπιθύμητες ενέργειες περιλαμβάνουν:
- Συμβάντα σχετιζόμενα με αυτοκτονίες
- Επιθετικότητα
- Συναισθηματική αστάθεια
- Ψύχωση
- Συγκοπή (λιποθυμία)
- Τρόμος
- Ημικρατνία
- Υπαισθησία
- Σπασμοί
- Αίσθημα παλμών
- Φλεβοκομβική ταχυκαρδία
- Παράταση διαστήματος QT
- Αυξημένη χολερυθρίνη αίματος
- Αλλεργικές αντιδράσεις
Σπάνιες (0,01-0,1% επίπτωση) ανεπιθύμητες ενέργειες όπως:
- Φαινόμενο του Ρεϊνό
- Μη φυσιολογικές / αυξημένες εξετάσεις ηπατικής λειτουργίας
- Ικτερός
- Ηπατίτιδα
- Βλάβη στο ήπαρ
- Οξεία ηπατική ανεπάρκεια
- Κατακράτηση ούρων
- Πριαπισμός[28]
- Πόνος γεννητικών οργάνων των αντρών
Υπερβολική δόση
[Επεξεργασία | επεξεργασία κώδικα]Η ατομοξετίνη είναι σχετικά μη τοξική σε υπερβολική δόση. Υπερδοσολογία με ένα φάρμακο που περιλαμβάνει πάνω από 1500 mg ατομοξετίνης δεν έχουν οδηγήσει σε θάνατο.[3] Τα πιο κοινά συμπτώματα υπερδοσολογίας περιλαμβάνουν:
- Γαστρεντερικά συμπτώματα
- Υπνηλία
- Ζάλη
- Τρόμος
- Αφύσικη συμπεριφορά
- Υπερδραστηριότητα
- Ανησυχία
- Ξηροστομία
- Ταχυκαρδία
- Υπέρταση
- Μυδρίαση
Λιγότερα κοινά συμπτώματα:[3]
- Επιληπτικές κρίσεις
- Παράταση διαστήματος QT
Η συνιστώμενη θεραπεία για την υπερδοσολογία ατομοξετίνης περιλαμβάνει τη χορήγηση ενεργού άνθρακα για την αποφυγή περαιτέρω απορρόφησης του φαρμάκου.[3]
Αλληλεπιδράσεις
[Επεξεργασία | επεξεργασία κώδικα]Η ατομοξετίνη είναι υπόστρωμα για το CYP2D6. Η ταυτόχρονη θεραπεία με αναστολέα του CYP2D6 όπως η βουπροπιόνη, η φλουοξετίνη ή η παροξετίνη έχει αποδειχθεί ότι αυξάνει την ατομοξετίνη στο πλάσμα κατά 100% ή περισσότερο, καθώς επίσης αυξάνουν τα επίπεδα της Ν -δεμεθυλατομοξετίνης και μειώνουν τα επίπεδα της 4-υδροξυτοτομοξετίνης στο πλάσμα κατά παρόμοιο βαθμό.[29][30][31]
Η ατομοξετίνη έχει βρεθεί ότι αναστέλλει άμεσα τον υποδοχέα καλίου hERG με IC50 6,3 μM, το οποίο έχει τη δυνατότητα να προκαλέσει αρρυθμία.[30][32] Έχει αναφερθεί η παράταση του QT με ατομοξετίνη σε θεραπευτικές δόσεις και σε υπερδοσολογία. Προτείνεται ότι η ατομοξετίνη δεν πρέπει να χρησιμοποιείται με άλλα φάρμακα που μπορεί να παρατείνουν το διάστημα QT, ταυτόχρονα με αναστολείς του CYP2D6 και να χρησιμοποιείται με προσοχή σε κακούς μεταβολιστές.
Άλλες αξιοσημείωτες αλληλεπιδράσεις φαρμάκων περιλαμβάνουν:[3]
- Αντιυπερτασικοί παράγοντες, καθώς η ατομοξετίνη ενεργεί ως έμμεσο συμπαθομιμητικό
- Συμπαθητικομιμητικά έμμεσης δράσης, όπως η ψευδοεφεδρίνη, οι αναστολείς επαναπρόσληψης νορεπινεφρίνης ή οι αναστολείς ΜΑΟ
- Άμεσα δρώντα συμπαθομιμητικά, όπως η φαινυλεφρίνη ή οι άλλοι αδρενεργικοί α1 αγωνιστές, συμπεριλαμβανομένων αγγειοσυσταλτικών όπως η δοβουταμίνη ή ισοπρεναλίνη και αγωνιστές του β2 αδρενοϋποδοχέα
- Φάρμακα με υψηλή περιεκτικότητα σε πρωτεΐνες πλάσματος: η ατομοξετίνη έχει τη δυνατότητα να εκτοπίσει αυτά τα φάρμακα από πρωτεΐνες πλάσματος που μπορεί να ενισχύσουν τις ανεπιθύμητες ή τοξικές τους επιδράσεις. In vitro, η ατομοξετίνη δεν επηρεάζει τη δέσμευση της ασπιρίνης, της δεσιπραμίνης, της διαζεπάμης, της παροξετίνης, της φαινυτοΐνης ή της βαρφαρίνης[5][33]
Φαρμακολογία
[Επεξεργασία | επεξεργασία κώδικα]Φαρμακοδυναμική
[Επεξεργασία | επεξεργασία κώδικα]Η ατομοξετίνη αναστέλλει τον προσυναπτικό μεταφορέα νορεπινεφρίνης (NET), εμποδίζοντας την επαναπρόσληψη νορεπινεφρίνης σε όλο τον εγκέφαλο, καθώς και την αναστολή της επαναπρόσληψης ντοπαμίνης σε συγκεκριμένες περιοχές του εγκεφάλου, όπως ο προμετωπιαίος φλοιός, όπου η έκφραση του μεταφορέα ντοπαμίνης (DAT) είναι ελάχιστη.[5] Σε αρουραίους, η ατομοξετίνη αύξησε τις συγκεντρώσεις κατεχολαμίνης στον προμετωπιαίο φλοιό χωρίς να μεταβάλλει τα επίπεδα ντοπαμίνης στο ραβδωτό σώμα ή στον επικλινή πυρήνα. Αντιθέτως, η μεθυλφαινιδάτη, ένας αναστολέας επαναπρόσληψης ντοπαμίνης, βρέθηκε να αυξάνει τα επίπεδα ντοπαμίνης στον προμετωπιαιό φλοιό, στο ραβδωτό σώμα και στον επικλινή πυρήνα ίδιο βαθμό.[34] Στα ποντίκια, η ατομοξετίνη βρέθηκε επίσης ότι αυξάνει τα επίπεδα της προμετωπιαίας κατεχολαμίνης χωρίς να επηρεάζει τα επίπεδα στο ραβδωτό σώμα και στον επικλινή πυρήνα.[35]
Το καθεστώς της ατομοξετίνης ως αναστολέας μεταφορέα σεροτονίνης (SERT) σε κλινικές δόσεις στον άνθρωπο είναι αβέβαιη. Μια μελέτη απεικόνισης PET σε πιθήκους ρήσους διαπίστωσε ότι η ατομοξετίνη καταλαμβάνει > 90% και> 85% των νευρικών NET και SERT, αντίστοιχα[36] Ωστόσο, και οι μελέτες μικροδιήθυσης σε ποντίκια και αρουραίους απέτυχαν να βρουν αύξηση της εξωκυτταρικής σεροτονίνης στον προμετωπιαίο φλοιό μετά από οξεία ή χρόνια θεραπεία με ατομοξετίνη.[34][35] Υποστηρίζοντας την επιλεκτικότητα της ατομοξετίνης, μια μελέτη σε ανθρώπους δεν διαπίστωσε επίδραση στην πρόσληψη σεροτονίνης στα αιμοπεταλία (δείκτης αναστολής SERT) και αναστολή των επιδράσεων της τυραμίνης στην πίεση (δείκτης αναστολής του ΝΕΤ).[37]
Η ατομοξετίνη έχει βρεθεί ότι δρα ως ανταγωνιστής υποδοχέα NMDA σε φλοιώδεις νευρώνες αρουραίου σε θεραπευτικές συγκεντρώσεις.[38][39] Προκαλεί ένα εξαρτώμενο από τη χρήση αποκλεισμό των ανοικτών διαύλων και η θέση δέσμευσής του αλληλεπικαλύπτεται με τη θέση σύνδεσης Mg2+. Ικανότητα της ατομοξετίνης να αυξήσει το ρυθμό ώσεων στον προμετωπιαίο φλοιό σε αναισθητοποιημένους αρουραίους δεν μπορούσε να αποκλειστεί από τον ανταγωνιστες των υποδοχέων D1 ή α2, αλλά θα μπορούσε να ενισχυθεί από ανταγονιστές των υποδοχέων NMDA ή α1, υποδηλώνοντας γλουταμινεργικό μηχανισμό.[40] Σε αρουραίους Sprague Dawley, η ατομοξετίνη μειώνει την περιεκτικότητα σε πρωτεΐνες NR2B χωρίς να αλλάζει τα επίπεδα μεταγραφής.[41] Η αφύσικη λειτουργία γλουταμινεργικών και NMDA υποδοχέων έχει εμπλακεί στην αιτιολογία της ΔΕΠΥ.[42][43]
Η ατομοξετίνη αναστέλλει επίσης αντιστρέψιμα ρεύματα GIRK στα ωοκύτταρα του Xenopus με τρόπο που εξαρτάται από τη συγκέντρωση, ανεξάρτητα από την τάση και ανεξάρτητα από το χρόνο.[44] Οι διαύλοι ιόντων Kir 3.1 / 3.2 ανοίγονται κατάντη μετά από Μ2, α2, D2 και Α1 διέγερση, καθώς και άλλων Gi-συζευγμένων υποδοχέων. Οι θεραπευτικές συγκεντρώσεις της ατομοξετίνης βρίσκονται εντός του εύρους αλληλεπίδρασης με GIRKs, ειδικά σε CYP2D6 κακούς μεταβολιστές. Δεν είναι γνωστό εάν αυτό συμβάλλει στις θεραπευτικές επιδράσεις της ατομοξετίνης στην ΔΕΠΥ.
Η 4-υδροξυτομοξετίνη, ο κύριος ενεργός μεταβολίτης της ατομοξετίνης σε εκτεταμένους μεταβολιστές CYP2D6, έχει βρεθεί ότι έχει υπο-μικρομοριακή συγγένεια για υποδοχείς οπιοειδών, ενεργώντας ως ανταγωνιστής στους μ-υποδοχείς οπιοειδών και μερικός αγωνιστής στους κ-υποδοχείς οπιοειδών.[45] Δεν είναι γνωστό εάν αυτή η δράση στον υποδοχέα κ-οπιοειδών οδηγεί σε ανεπιθύμητες ενέργειες που σχετίζονται με το ΚΝΣ.
Φαρμακοκινητική
[Επεξεργασία | επεξεργασία κώδικα]Η από του στόματος ατομοξετίνη απορροφάται γρήγορα και πλήρως.[5] Ο μεταβολισμός πρώτης διέλευσης από το ήπαρ εξαρτάται από τη δραστηριότητα του CYP2D6, με αποτέλεσμα την απόλυτη βιοδιαθεσιμότητα 63% για εκτεταμένους μεταβολιστές και 94% για τους κακούς μεταβολιστές. Η μέγιστη συγκέντρωση στο πλάσμα επιτυγχάνεται σε 1-2 ώρες. Εάν ληφθεί με τροφή, η μέγιστη συγκέντρωση στο πλάσμα μειώνεται κατά 10-40% και καθυστερεί το t max κατά 1 ώρα. Φάρμακα που επηρεάζουν το γαστρικό pH δεν επηρεάζουν τη στοματική βιοδιαθεσιμότητα.[15]
Η ατομοξετίνη έχει όγκο κατανομής 0,85 L/kg, με περιορισμένη κατανομή στα ερυθρά αιμοσφαίρια.[5] Συνδέεται σε μεγάλο βαθμό με τις πρωτεΐνες του πλάσματος (98,7%), κυρίως αλβουμίνη, μαζί με την α 1 όξινη γλυκοπρωτεΐνη (77%) και IgG (15%).[33] Ο μεταβολίτης της Ν -δεμεθυλατομοξετίνς δεσμεύεται κατά 99,1% στις πρωτεΐνες του πλάσματος, ενώ η 4-υδροξυατομοξετίνη δεσμεύεται μόνο στο 66,6%.
Ο χρόνος ημιζωής της ατομοξετίνης ποικίλλει ευρέως μεταξύ των ατόμων, με μέσο εύρος 4,5 έως 19 ώρες.[5][6] Καθώς η ατομοξετίνη μεταβολίζεται από το CYP2D6, η έκθεση μπορεί να αυξηθεί 10 φορές στους φτωχούς μεταβολιστές του CYP2D6.
Η ατομοξετίνη, η Ν -δεσμμεθυλατομοξετίνη και η 4-υδροξυτοτομοξετίνη παράγουν ελάχιστη έως καθόλου αναστολή των CYP1A2 και CYP2C9, αλλά αναστέλλουν το CYP2D6 σε ανθρώπινα ηπατικά μικροσώματα σε συγκεντρώσεις μεταξύ 3,6-17 μmol / L. Οι συγκεντρώσεις στο πλάσμα της 4-υδροξυτοτομοξετίνης και της Ν -δεμεθυλατομοξετίνης σε σταθερή κατάσταση είναι 1,0% και 5% της ατομοξετίνης σε εκτεταμένους μεταβολιστές CYP2D6, και είναι 5% και 45% αυτής της ατομοξετίνης σε κακούς μεταβολιστές CYP2D6.[15]
Η ατομοξετίνη απεκκρίνεται αμετάβλητη στα ούρα σε <3% τόσο στους εκτεταμένους όσο και στους φτωχούς μεταβολιστές CYP2D6, με> 96% και 80% της συνολικής δόσης να απεκκρίνεται στα ούρα, αντίστοιχα.[5] Τα κλάσματα που απεκκρίνονται στα ούρα ως 4-υδροξυατομοξετίνη και ως γλυκουρονίδιο της αντιπροσωπεύουν το 86% μιας δεδομένης δόσης σε εκτεταμένους μεταβολιστές, αλλά μόνο το 40% στους κακούς μεταβολιστές. Οι φτωχοί μεταβολιστές του CYP2D6 εκκρίνουν μεγαλύτερες ποσότητες δευτερευόντων μεταβολιτών, συγκεκριμένα Ν -δεμεθυλατομοξετίνη και 2-υδροξυμεθυλατομοξετίνη και τα συζεύγματά τους.

Φαρμακογονιδιωματική
[Επεξεργασία | επεξεργασία κώδικα]Οι Κινέζοι ενήλικες ομόζυγοι για το υποδραστικό αλληλόμορφο CYP2D6 * 10 βρέθηκε ότι παρουσιάζουν δύο φορές υψηλότερες AUCs και 1,5 φορές υψηλότερες μέγιστες συγκεντρώσεις στο πλάσμα σε σύγκριση με τους εκτεταμένους μεταβολιστές.[5]
Χημεία
[Επεξεργασία | επεξεργασία κώδικα]Η ατομοξετίνη, ή (-)-μεθυλ[(3R)-3-(2-μεθυλοφαινοξυ)-3-φαινυλοπροπυλαμίνη, είναι μια λευκή, κοκκώδης σκόνη που είναι εξαιρετικά διαλυτή στο νερό.
-
Κάψουλα Strattera 60 mg
-
Κάψουλα Strattera 60 mg με λογότυπο της Lilly
Ανίχνευση σε βιολογικά υγρά
[Επεξεργασία | επεξεργασία κώδικα]Η ατομοξετίνη μπορεί να ποσοτικοποιηθεί στο πλάσμα, στον ορό ή στο αίμα, προκειμένου να διακριθούν οι εκτεταμένοι έναντι των φτωχών μεταβολιστών σε εκείνους που λαμβάνουν το φάρμακο θεραπευτικά, να επιβεβαιώσουν τη διάγνωση σε πιθανά θύματα δηλητηρίασης ή να βοηθήσουν στην ιατροδικαστική έρευνα σε περίπτωση θανατηφόρας υπερδοσολογίας.[46]
Ιστορία
[Επεξεργασία | επεξεργασία κώδικα]Η ατομοξετίνη κατασκευάζεται, διατίθεται στο εμπόριο και πωλείται στις Ηνωμένες Πολιτείες ως το υδροχλωρικό άλας (ατομοξετίνη HCl) με την επωνυμία Strattera από την Eli Lilly και Σία, την εταιρεία που κατέθεσε πρώτη δίπλωμα ευρεσιτεχνίας και τρέχοντα κάτοχο διπλωμάτων ευρεσιτεχνίας των ΗΠΑ. Η ατομοξετίνη προοριζόταν αρχικά να αναπτυχθεί ως αντικαταθλιπτικό, αλλά βρέθηκε ότι δεν ήταν επαρκώς αποτελεσματική για τη θεραπεία της κατάθλιψης. Ωστόσο, αποδείχθηκε αποτελεσματική για τη ΔΕΠΥ και εγκρίθηκε από το FDA το 2002, για τη θεραπεία της ΔΕΠΥ. Το δίπλωμα ευρεσιτεχνίας του έληξε τον Μάιο του 2017.[47] Στις 12 Αυγούστου 2010, η Lilly έχασε μια αγωγή που αμφισβήτησε το δίπλωμα ευρεσιτεχνίας της για το Strattera, αυξάνοντας την πιθανότητα νωρίτερης εισόδου ενός γενόσημου προϊόντος στην αμερικανική αγορά.[48] Την 1η Σεπτεμβρίου 2010, η Sun Pharmaceuticals ανακοίνωσε ότι θα αρχίσει να κατασκευάζει ένα γενόσημο στις Ηνωμένες Πολιτείες.[49] Ωστόσο, σε μια τηλεδιάσκεψη της 29ης Ιουλίου 2011, ο Πρόεδρος της Sun Pharmaceutical δήλωσε ότι "η Lilly κέρδισε την εν λόγω ένσταση κατόπιν έφεσης, γι 'αυτό νομίζω ότι [το γενόσημο Strattera] αναβλήθηκε."[50]
Το 2017 ο FDA ενέκρινε την παραγωγή γενόσημης ατομοξετίνης από τέσσερις φαρμακευτικές εταιρείες.[51]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ «Atomoxetine (Strattera) Use During Pregnancy». Drugs.com. 22 Αυγούστου 2019. Ανακτήθηκε στις 7 Φεβρουαρίου 2020.
- ↑ 2,0 2,1 2,2 2,3 2,4 «atomoxetine (Rx) – Strattera». Medscape Reference. WebMD. Αρχειοθετήθηκε από το πρωτότυπο στις 10 Νοεμβρίου 2013. Ανακτήθηκε στις 10 Νοεμβρίου 2013.
- ↑ 3,00 3,01 3,02 3,03 3,04 3,05 3,06 3,07 3,08 3,09 3,10 3,11 3,12 3,13 «Strattera (atomoxetine hydrochloride)». TGA eBusiness Services. Eli Lilly Australia Pty. Limited. 21 Αυγούστου 2013. Αρχειοθετήθηκε από το πρωτότυπο στις 6 Απριλίου 2017. Ανακτήθηκε στις 10 Νοεμβρίου 2013.
- ↑ 4,0 4,1 4,2 4,3 4,4 «ATOMOXETINE HYDROCHLORIDE capsule [Mylan Pharmaceuticals Inc.]». DailyMed. Mylan Pharmaceuticals Inc. Οκτωβρίου 2011. Αρχειοθετήθηκε από το πρωτότυπο στις 10 Νοεμβρίου 2013. Ανακτήθηκε στις 10 Νοεμβρίου 2013.
- ↑ 5,00 5,01 5,02 5,03 5,04 5,05 5,06 5,07 5,08 5,09 «Clinical pharmacokinetics of atomoxetine». Clinical Pharmacokinetics 44 (6): 571–90. 2005. doi:. PMID 15910008.
- ↑ 6,0 6,1 «Atomoxetine pharmacogenetics: associations with pharmacokinetics, treatment response and tolerability». Pharmacogenomics 16 (13): 1513–20. 2015. doi:. PMID 26314574.
- ↑ 7,0 7,1 7,2 7,3 «Atomoxetine Hydrochloride Monograph for Professionals». Drugs.com (στα Αγγλικά). American Society of Health-System Pharmacists. Αρχειοθετήθηκε από το πρωτότυπο στις 4 Απριλίου 2019. Ανακτήθηκε στις 22 Μαρτίου 2019.
- ↑ 8,0 8,1 «A systematic review of combination therapy with stimulants and atomoxetine for attention-deficit/hyperactivity disorder, including patient characteristics, treatment strategies, effectiveness, and tolerability». Journal of Child and Adolescent Psychopharmacology 23 (3): 179–93. April 2013. doi:. PMID 23560600.
- ↑ «Parent's Medication Guide: ADHD». American Psychiatric Association (Guidelines (Tertiary source)). American Psychiatric Association & American Academy of Child and Adolescent Psychiatry (AACAP). Ιουνίου 2013. Αρχειοθετήθηκε από το πρωτότυπο στις 2 Φεβρουαρίου 2017. Ανακτήθηκε στις 1 Ιανουαρίου 2017.
Though not FDA-approved for combined treatment, atomoxetine (Strattera) is sometimes used in conjunction with stimulants as an off-label combination therapy.
- ↑ «The Top 300 of 2021». ClinCalc. Ανακτήθηκε στις 18 Φεβρουαρίου 2021.
- ↑ «Atomoxetine Hydrochloride - Drug Usage Statistics». ClinCalc. Αρχειοθετήθηκε από το πρωτότυπο στις 9 Ιουλίου 2018. Ανακτήθηκε στις 18 Φεβρουαρίου 2021.
- ↑ 12,0 12,1 British national formulary : BNF 76 (76 έκδοση). Pharmaceutical Press. 2018. σελίδες 344–345. ISBN 9780857113382.
- ↑ 13,0 13,1 «Atomoxetine Pregnancy and Breastfeeding Warnings». Drugs.com (στα Αγγλικά). Αρχειοθετήθηκε από το πρωτότυπο στις 22 Μαρτίου 2019. Ανακτήθηκε στις 3 Μαρτίου 2019.
- ↑ 14,0 14,1 «Pharmacological Treatment of Attention Deficit Hyperactivity Disorder During Pregnancy and Lactation». Pharmaceutical Research 35 (3): 46. February 2018. doi:. PMID 29411149.
- ↑ 15,0 15,1 15,2 15,3 «Strattera (atomoxetine) Capsules for Oral Use». DailyMed.gov. Eli Lilly and Company. 29 Ιανουαρίου 2020. Αρχειοθετήθηκε από το πρωτότυπο στις 7 Ιουνίου 2018. Ανακτήθηκε στις 26 Φεβρουαρίου 2020.
- ↑ «Atomoxetine is a second-line medication treatment option for ADHD». Evidence-Based Mental Health 17 (4): 108. November 2014. doi:. PMID 25165169. Αρχειοθετήθηκε από το πρωτότυπο στις 8 March 2016. https://web.archive.org/web/20160308115106/http://ebmh.bmj.com/content/17/4/108. Ανακτήθηκε στις 8 March 2016.
- ↑ Kooij, JJS (2013). Adult ADHD Diagnostic Assessment and Treatment. Springer London. ISBN 978-1-4471-4137-2.
- ↑ «NIMH » Attention Deficit Hyperactivity Disorder». NIMH » Home. Αυτό το λήμμα αυτό ενσωματώνει υλικό από ιστότοπους ή έγγραφα του Εθνικού Ινστιτούτου Ψυχικής Υγείας, το οποίο είναι πλέον κοινό κτήμα. Αρχειοθετήθηκε από το πρωτότυπο στις 25 Δεκεμβρίου 2016. Ανακτήθηκε στις 21 Ιουλίου 2018.
- ↑ «NIMH » Mental Health Medications». NIMH » Home. Αρχειοθετήθηκε από το πρωτότυπο στις 6 Απριλίου 2019. Ανακτήθηκε στις 17 Μαΐου 2019.
- ↑ The Maudsley prescribing guidelines in psychiatry. West Sussex: Wiley-Blackwell. 2012. ISBN 978-0-470-97948-8.
- ↑ «The use of stimulants and atomoxetine in adults with comorbid ADHD and bipolar disorder». Expert Opinion on Pharmacotherapy 16 (14): 2193–204. 2015. doi:. PMID 26364896.
- ↑ Autism Spectrum Disorder Parents Medication Guide (PDF). Washington, DC: American Academy of Child and Adolescent Psychiatry. 2016. σελ. 13.
Atomoxetine (Strattera) has also been researched in controlled studies for treatment of ADHD in children with autism, and showed some improvements, particularly for hyperactivity and impulsivity
- ↑ Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (3rd έκδοση). New York: McGraw-Hill Medical. 2015. ISBN 9780071827706.
- ↑ «Safety of 80 antidepressants, antipsychotics, anti-attention-deficit/hyperactivity medications and mood stabilizers in children and adolescents with psychiatric disorders: a large scale systematic meta-review of 78 adverse effects». World Psychiatry 19 (2): 214–232. June 2020. doi:. PMID 32394557.
- ↑ «Atomoxetine and suicidality in children and adolescents». Australian Prescriber 36 (5): σελ. 166. October 2013. Αρχειοθετήθηκε από το πρωτότυπο στις 10 November 2013. https://web.archive.org/web/20131110153948/http://www.australianprescriber.com/magazine/36/5/166/9. Ανακτήθηκε στις 10 November 2013.
- ↑ «Strattera 10mg, 18mg, 25mg, 40mg, 60mg, 80mg or 100mg hard capsules». electronic Medicines Compendium. 28 Μαΐου 2013. Αρχειοθετήθηκε από το πρωτότυπο στις 10 Νοεμβρίου 2013. Ανακτήθηκε στις 10 Νοεμβρίου 2013.
- ↑ «Strattera Product Insert». Ανακτήθηκε στις 8 Δεκεμβρίου 2013.
- ↑ «Strattera Medication Guide» (PDF). U.S. Food and Drug Administration (FDA). Eli Lilly and Company. 2003. Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 10 Δεκεμβρίου 2013. Ανακτήθηκε στις 17 Δεκεμβρίου 2013.
- ↑ «Evaluation of a Potential Metabolism-Mediated Drug-Drug Interaction Between Atomoxetine and Bupropion in Healthy Volunteers». Journal of Pharmacy & Pharmaceutical Sciences 19 (2): 198–207. April–June 2016. doi:. PMID 27518170.
- ↑ 30,0 30,1 «Cardiovascular side effects of atomoxetine and its interactions with inhibitors of the cytochrome p450 system». Case Reports in Medicine 2011: 952584. 2011. doi:. PMID 21765848.
- ↑ «Effect of potent CYP2D6 inhibition by paroxetine on atomoxetine pharmacokinetics». Journal of Clinical Pharmacology 42 (11): 1219–27. November 2002. doi:. PMID 12412820. https://archive.org/details/sim_journal-of-clinical-pharmacology_2002-11_42_11/page/1219.
- ↑ «Selective noradrenaline reuptake inhibitor atomoxetine directly blocks hERG currents». British Journal of Pharmacology 156 (2): 226–36. January 2009. doi:. PMID 19154426.
- ↑ 33,0 33,1 «21-411 Strattera Clinical Pharmacology Biopharmaceutics Review Part 2» (PDF). U.S. Food and Drug Administration (FDA). Αρχειοθετήθηκε από το πρωτότυπο (PDF) στις 1 Μαρτίου 2017. Ανακτήθηκε στις 6 Αυγούστου 2017.
- ↑ 34,0 34,1 «Atomoxetine increases extracellular levels of norepinephrine and dopamine in prefrontal cortex of rat: a potential mechanism for efficacy in attention deficit/hyperactivity disorder». Neuropsychopharmacology 27 (5): 699–711. November 2002. doi:. PMID 12431845.
- ↑ 35,0 35,1 «Effects of acute and chronic administration of atomoxetine and methylphenidate on extracellular levels of noradrenaline, dopamine and serotonin in the prefrontal cortex and striatum of mice». Journal of Neurochemistry 114 (1): 259–70. July 2010. doi:. PMID 20403082.
- ↑ «Clinical doses of atomoxetine significantly occupy both norepinephrine and serotonin transports: Implications on treatment of depression and ADHD». NeuroImage 86: 164–71. February 2014. doi:. PMID 23933039. «The noradrenergic action also exerts an important clinical effect in different antidepressant classes such as desipramine and nortriptyline (tricyclics, prevalent noradrenergic effect), reboxetine and atomoxetine (relatively pure noradrenergic reuptake inhibitor (NRIs)), and dual action antidepressants such as the serotonin noradrenaline reuptake inhibitors (SNRIs), the noradrenergic and dopaminergic reuptake inhibitor (NDRI) bupropion, and other compounds (e.g., mianserin, mirtazapine), which enhance the noradrenergic transmission».
- ↑ «Clinical pharmacology of tomoxetine, a potential antidepressant». The Journal of Pharmacology and Experimental Therapeutics 232 (1): 139–43. January 1985. PMID 3965689.
- ↑ «Atomoxetine acts as an NMDA receptor blocker in clinically relevant concentrations». British Journal of Pharmacology 160 (2): 283–91. May 2010. doi:. PMID 20423340.
- ↑ «Inhibition of the NMDA and AMPA receptor channels by antidepressants and antipsychotics». Brain Research 1660: 58–66. April 2017. doi:. PMID 28167075.
- ↑ «Psychostimulants and atomoxetine alter the electrophysiological activity of prefrontal cortex neurons, interaction with catecholamine and glutamate NMDA receptors». Psychopharmacology 232 (12): 2191–205. June 2015. doi:. PMID 25572531.
- ↑ «Atomoxetine affects transcription/translation of the NMDA receptor and the norepinephrine transporter in the rat brain--an in vivo study». Drug Design, Development and Therapy 7: 1433–46. 2013. doi:. PMID 24348020.
- ↑ «Glutamate/glutamine and neuronal integrity in adults with ADHD: a proton MRS study». Translational Psychiatry 4 (3): e373. March 2014. doi:. PMID 24643164.
- ↑ «Attention deficit hyperactivity disorder and N-methyl-D-aspartate (NMDA) dysregulation». Current Pharmaceutical Design 20 (32): 5180–5. 2014. doi:. PMID 24410567.
- ↑ «Inhibition of G-protein-activated inwardly rectifying K+ channels by the selective norepinephrine reuptake inhibitors atomoxetine and reboxetine». Neuropsychopharmacology 35 (7): 1560–9. June 2010. doi:. PMID 20393461.
- ↑ «Synthesis and biological evaluation of the major metabolite of atomoxetine: elucidation of a partial kappa-opioid agonist effect». Bioorganic & Medicinal Chemistry Letters 14 (15): 4083–5. August 2004. doi:. PMID 15225731.
- ↑ Baselt, Randall C. (2008). Disposition of Toxic Drugs and Chemicals in Man (8th έκδοση). Foster City, CA: Biomedical Publications. σελίδες 118–20. ISBN 978-0-931890-08-6.
- ↑ «Patent and Exclusivity Search Results». Electronic Orange Book. U.S. Food and Drug Administration (FDA). Αρχειοθετήθηκε από το πρωτότυπο στις 22 Μαρτίου 2012. Ανακτήθηκε στις 26 Απριλίου 2009.
- ↑ «Drugmaker Eli Lilly loses patent case over ADHD drug, lowers revenue outlook». Chicago Tribune. http://www.chicagotribune.com/business/sns-ap-us-eli-lilly-patent,0,7016147.story.[νεκρός σύνδεσμος]
- ↑ «Sun Pharma receives USFDA approval for generic Strattera capsules». International Business Times. Αρχειοθετήθηκε από το πρωτότυπο στις 7 April 2011. https://web.archive.org/web/20110407100949/http://www.ibtimes.com/articles/48022/20100901/sun-pharma-usfda-strattera-capsules-eli-lilly-atomoxetine-hydrochloride-attention-deficit-hyperactiv.htm.
- ↑ «Sun Pharma Q1 2011-12 Earnings Call Transcript 10.00 am, July 29, 2011». Αρχειοθετήθηκε από το πρωτότυπο στις 29 September 2011. https://web.archive.org/web/20110929013747/http://www.sunpharma.com/images/finance/FY12%20Q1%20Earnings%20Call%20Transcript.pdf.
- ↑ (May 30, 2017). FDA approves first generic Strattera for the treatment of ADHD. Δελτίο τύπου.
Εξωτερικοί σύνδεσμοι
[Επεξεργασία | επεξεργασία κώδικα]- «Atomoxetine». Drug Information Portal. U.S. National Library of Medicine.
- «Strattera (Atomoxetine) - Published Studies». Druglib. Αρχειοθετήθηκε από το πρωτότυπο στις 14 Μαρτίου 2008. Ανακτήθηκε στις 16 Ιουνίου 2021.