Καρβοξυλίωση
Η καρβοξυλίωση (Carboxylation) είναι μια χημική αντίδραση κατά την οποία παράγεται ένα καρβοξυλικό οξύ με επεξεργασία ενός υποστρώματος με διοξείδιο του άνθρακα.[1] Η αντίθετη αντίδραση είναι η αποκαρβοξυλίωση (decarboxylation). Στη χημεία, ο όρος ενανθράκωση (carbonation) χρησιμοποιείται μερικές φορές συνώνυμα με την καρβοξυλίωση, ειδικά όταν εφαρμόζεται στην αντίδραση καρβανιονικών αντιδραστηρίων με CO2. Γενικότερα, η ενανθράκωση συνήθως περιγράφει την παραγωγή ανθρακικών.[2]
Οργανική χημεία
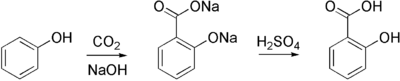
[Επεξεργασία | επεξεργασία κώδικα]Η καρβοξυλίωση είναι μια τυπική μετατροπή στην οργανική χημεία.[3] Συγκεκριμένα η ενανθράκωση (δηλαδή η καρβοξυλίωση) των αντιδραστηρίων Grignard και των ενώσεων οργανολιθίου είναι ένας κλασικός τρόπος μετατροπής οργανικών αλογονιδίων σε καρβοξυλικά οξέα.[4] Το σαλικυλικό νάτριο, πρόδρομο της ασπιρίνης, παρασκευάζεται εμπορικά με επεξεργασία φαινολικού νατρίου (το άλας νατρίου της φαινόλης) με διοξείδιο του άνθρακα σε υψηλή πίεση (100 atm ) και υψηλή θερμοκρασία (390 K) – μια μέθοδος γνωστή ως αντίδραση Kolbe-Schmitt. Η οξίνιση του προκύπτοντος σαλικυλικού άλατος δίνει σαλικυλικό οξύ.
Πολλές λεπτομερείς διαδικασίες περιγράφονται στο περιοδικό Organic Syntheses.[5][6][7] Οι καταλύτες καρβοξυλίωσης περιλαμβάνουν Ν-ετεροκυκλικά καρβένια [8] και καταλύτες με βάση τον άργυρο.[9]
Η καρβοξυλίωση στη βιοχημεία
[Επεξεργασία | επεξεργασία κώδικα]Η ζωή με βάση τον άνθρακα προέρχεται από την καρβοξυλίωση που συνδέει το ατμοσφαιρικό διοξείδιο του άνθρακα με ένα σάκχαρο. Η διαδικασία συνήθως καταλύεται από το ένζυμο RuBisCO (καρβοξυλάση/οξυγενάση της 1,5-διφωσφορικής ριβουλόζης), που είναι πιθανώς η μόνη πιο άφθονη πρωτεΐνη στη Γη.[10][11][12]


Πολλές καρβοξυλάσες, συμπεριλαμβανομένων των καρβοξυλάση του ακετυλοσυνένζυμου Α (Acetyl-CoA carboxylase), καρβοξυλάση του μεθυλοκροτονυλοσυνένζυμου Α (Methylcrotonyl-CoA carboxylase), καρβοξυλάση του προπιονυλοσυνένζυμου Α (Propionyl-CoA carboxylase) και πυροσταφυλικής καρβοξυλάσης (Pyruvate carboxylase) απαιτούν βιοτίνη ως συμπαράγοντα. Αυτά τα ένζυμα εμπλέκονται σε διάφορες βιογονικές οδούς.[13] Στο σχήμα EC, τέτοιες καρβοξυλάσες ταξινομούνται στην EC 6.3.4, "Άλλες λιγάσες άνθρακα-αζώτου". Ένα άλλο παράδειγμα είναι η μεταμεταφραστική τροποποίηση υπολειμμάτων γλουταμινικού οξέος, σε γ-καρβοξυγλουταμινικό, σε πρωτεΐνες. Εμφανίζεται κυρίως σε πρωτεΐνες που εμπλέκονται στον καταρράκτη πήξης του αίματος, συγκεκριμένα στους παράγοντες II, VII, IX και X, στην πρωτεΐνη C και στην πρωτεΐνη S, καθώς και σε ορισμένες πρωτεΐνες των οστών. Αυτή η τροποποίηση απαιτείται για να λειτουργήσουν αυτές οι πρωτεΐνες. Η καρβοξυλίωση λαμβάνει χώρα στο ήπαρ και εκτελείται από τη γ-γλουταμυλοκαρβοξυλάση (γ-glutamyl carboxylase, GGCX).[14] Η GGCX απαιτεί βιταμίνη Κ ως συμπαράγοντα και εκτελεί την αντίδραση με διεργαστικό τρόπο.[15]Το γ-καρβοξυγλουταμικό δεσμεύει το ασβέστιο, το οποίο είναι απαραίτητο για τη δράση του.[16] Παραδείγματος χάρη, στην προθρομβίνη (prothrombin), η δέσμευση ασβεστίου επιτρέπει στην πρωτεΐνη να συσχετιστεί με την κυτταρική μεμβράνη στα αιμοπετάλια, φέρνοντάς την σε άμεση γειτνίαση με τις πρωτεΐνες που διασπούν την προθρομβίνη σε ενεργή θρομβίνη μετά από τραυματισμό.[17]
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ "Carboxylation: The introduction of a carboxyl group into a molecule or compound to form a carboxylic acid or a carboxylate; an instance of this."Oxford English Dictionary. Oxford University Press. 2018.
- ↑ "Carbonation: Impregnation or treatment with carbon dioxide; conversion into a carbonate."Oxford English Dictionary. Oxford University Press. 2018.
- ↑ Braunstein, Pierre; Matt, Dominique; Nobel, Dominique (August 1988). «Reactions of Carbon Dioxide with Carbon-Carbon Bond Formation Catalyzed by Transition-Metal Complexes». Chemical Reviews 88 (5): 747–764. doi:.
- ↑ A. M. Appel (2013). «Frontiers, Opportunities, and Challenges in Biochemical and Chemical Catalysis of CO2 Fixation». Chem. Rev. 113 (8): 6621–6658. doi:. PMID 23767781.
- ↑ Akira Yanagisawa; Katsutaka Yasue; Hisashi Yamamoto (1997). «Regio- and Stereoselective Carboxylation of Allylic Barium Reagents: (E)-4,8-Dimethyl-3,7-Nonadienoic Acid». Organic Syntheses 74: 178. doi:.
- ↑ H. Koch; W. Haaf (1964). «1-Adamantanecarboxylic Acid». Organic Syntheses 44: 1. doi:.
- ↑ W. Haaf (1966). «1-Methylcyclohexanecarboxylic Acid». Organic Syntheses 46: 72. doi:.
- ↑ Zhang Liang (2013). «N-Heterocyclic carbene (NHC)–copper-catalysed transformations of carbon dioxide». Chemical Science 4 (9): 3395. doi:.
- ↑ K. Sekine; T. Yamada (2016). «Silver-catalyzed carboxylation». Chem. Soc. Rev. 45 (16): 4524–4532. doi:. PMID 26888406.
- ↑ «Enhanced translation of a chloroplast-expressed RbcS gene restores small subunit levels and photosynthesis in nuclear RbcS antisense plants». Proc. Natl. Acad. Sci. U.S.A. 101 (16): 6315–20. April 2004. doi:. PMID 15067115. Bibcode: 2004PNAS..101.6315D. «(Rubisco) is the most prevalent enzyme on this planet, accounting for 30–50% of total soluble protein in the chloroplast;».
- ↑ «Rubiscolytics: fate of Rubisco after its enzymatic function in a cell is terminated». J. Exp. Bot. 59 (7): 1615–24. 2008. doi:. PMID 17975207. https://boris.unibe.ch/30426/1/2008_JExpBot_59_1615.pdf.
- ↑ Raven, John A. (April 2013). «Rubisco: still the most abundant protein of Earth?». New Phytologist 198 (1): 1–3. doi:. PMID 23432200.
- ↑ «Biotin – Fact Sheet for Health Professionals». Office of Dietary Supplements, US National Institutes of Health. 8 Δεκεμβρίου 2017. Ανακτήθηκε στις 25 Φεβρουαρίου 2018.
- ↑ OMIM - gamma-glutamyl carboxylase, contributed by McKusick VA, last updated October 2004 [1]
- ↑ «Processive post-translational modification. Vitamin K-dependent carboxylation of a peptide substrate». J. Biol. Chem. 270 (51): 30491–8. 1995. doi:. PMID 8530480.
- ↑ «Direct identification of the calcium-binding amino acid, gamma-carboxyglutamate, in mineralized tissue». Proc. Natl. Acad. Sci. U.S.A. 72 (10): 3925–9. 1975. doi:. PMID 1060074. Bibcode: 1975PNAS...72.3925H.
- ↑ Berg JM, Tymoczko JL, Stryer L. Biochemistry, 5th ed. New York: W. H. Freeman and Company, 2002.